| Sepsis | ||
|---|---|---|

La activación de la cascada de la coagulación causada por las citocinas genera microtrombos capilares y al final la isquemia de diversos órganos.
|
||
| Especialidad | infectología | |
Infección.
Se llama infección a todo proceso patológico secundario a la invasión por microorganismos patógenos o potencialmente patógenos de un tejido, líquido o cavidad anatómica que en condiciones normales deben permanecer estériles. Sin embargo, está definición no es perfecta, ya que, por ejemplo, el colon no es estéril y una infección por Clostridium difficile se puede generar allí. Las manifestaciones de la infección por este germen no se relacionan con la invasión, sino con la exotoxina que produce.
Sepsis.
Sepsis, hasta el año 2015, significaba, de acuerdo con los expertos, una infección con manifestaciones de respuesta inflamatoria sistémica (SRIS), como fiebre o hipotermia, taquicardia, taquipnea, leucocitosis o leucopenia, entre otras. Desde el año 2017, según los mismos expertos, el término sepsis se define como la disfunción orgánica causada por una respuesta anómala del huésped a la infección que supone una amenaza para la supervivencia. En cuanto a la disfunción orgánica, con fines de operatividad clínica puede ser definida como un aumento de dos puntos o más en el sistema de medición SOFA (Sequential [Sepsis-related] Organ Failure Assessment o Evaluación Secuencial de la Insuficiencia Orgánica —relacionada con la sepsis—), lo que se asocia con una mortalidad hospitalaria mayor del diez por ciento y por ende merece una respuesta rápida y adecuada.
Sepsis grave.
El término «sepsis grave», hasta el año 2015, significaba, de acuerdo con los expertos, la presencia de sepsis en asociación con manifestaciones de disfunción orgánica o de hipoperfusión tisular, como hipoxemia, oliguria, acidosis láctica, elevación de enzimas hepáticas, alteración mental y trastorno de la coagulación, entre otras. Desde el año 2015, según los mismos expertos, se considera un término redundante (la sepsis siempre es grave).
Choque séptico.
El choque séptico, hasta el año 2015, significaba, de acuerdo con los expertos, una sepsis con insuficiencia circulatoria por hipotensión arterial persistente (presión arterial media o PAM inferior a 60 mmHg) pese a una terapia con líquidos correcta. Desde el año 2015, según los mismos expertos, el choque séptico es un tipo de sepsis que se acompaña de anomalías circulatorias, celulares y metabólicas lo bastante profundas como para aumentar de manera sustancial la mortalidad.
Los pacientes con choque séptico son aquellos con sepsis con hipotensión persistente que requiere vasopresores para mantener la presión arterial media (PAM) ≥ 65 mmHg y un nivel de lactato sérico mayor de 2 mmol/L (18 mg/dL) a pesar de la reposición adecuada de volumen. Cuando se cumple ese criterio la mortalidad hospitalaria supera el 40 %.
Síndrome de disfunción multiorgánica por sepsis.
Este síndrome define el compromiso de distintos órganos en un paciente con choque séptico.
Síndrome de respuesta inflamatoria sistemica.
El llamado síndrome de respuesta inflamatoria sistémica (SIRS) es un proceso inflamatorio que se encuentra asociado al menos con 2 de las siguientes manifestaciones clínicas: temperatura corporal > 38 °C o < 36 °C; frecuencia cardíaca > 90 latidos por minuto; frecuencia respiratoria > 20 respiraciones por minuto o evidencia de hiperventilación con una PaCO2 < 32 mmHg; recuento de leucocitos en sangre periférica > 12 000/mm³ o < 4000/mm³, o con presencia de neutrófilos inmaduros (bandas) ≥ 10 %. Cuando el SIRS es el resultado de un proceso infeccioso se denomina sepsis. La conferencia de consenso de expertos en el año 2001 evaluó esta definición y destacó que los criterios del SIRS no son muy sensibles ni específicos y propone mejorarlo de tal forma que refleje un proceso infeccioso con respuesta generalizada del individuo.
Síndrome de respuesta antiinflamatoria compensatoria.
El síndrome de respuesta antiinflamatoria compensatoria, se caracteriza por disminución en la expresión del HLA-DR en monocitos, apoptosis en linfocitos y predominio de la respuesta Th2 sobre Th1.
Sepsis neonatal.
Sepsis neonatal es el término utilizado para describir cualquier infección bacteriana sistémica documentada por un hemocultivo positivo en el primer mes de vida.
Clasificación.
La sepsis puede clasificarse de diferentes formas, según su gravedad o por tipos específicos.
Según su gravedad.
Se distinguen tres formas: sepsis no complicada, sepsis grave y choque séptico. La enfermedad en un paciente puede progresar desde una infección y luego a través de las tres etapas mencionadas, desarrollar una falla en múltiples órganos lo que puede llevarlo finalmente a su muerte.
- La sepsis no complicada suele ser causada por una gripe u otras infecciones virales, por gastroenteritis o por un absceso dental; se trata de una forma muy común (afecta a millones de personas por año) que en la mayor parte de los casos no requiere tratamiento hospitalario.
- La sepsis grave se estima que en América del Norte se producen más de 750 000 casos anuales, con estimaciones similares para Europa, y todos esos casos deben ser tratados en el hospital. Esa etapa se desarrolla cuando la sepsis se produce en combinación con problemas de uno o más órganos vitales, como el corazón, los riñones, los pulmones o el hígado, y a causa de esos problemas las personas con sepsis grave tienen más probabilidades de morir (la tasa de mortalidad es de alrededor del treinta al treinta y cinco por ciento) que las afectadas por sepsis sin complicaciones.
- El choque séptico se produce cuando la sepsis se complica con un descenso de la presión arterial que no responde al tratamiento estándar (administración de líquidos) y, como ya se dijo, conduce a problemas en uno o más de los órganos vitales. En esa situación el cuerpo no recibe la cantidad de oxígeno que necesita para funcionar adecuadamente y se utilizan medicamentos llamados vasopresores para aumentar la presión arterial. Los pacientes con choque séptico están muy graves y necesitan ser internados cuanto antes en una unidad de cuidados intensivos. Sin embargo, aun con tratamiento activo en esa unidad, la tasa de mortalidad se aproxima al cincuenta por ciento.
Según tipos específicos.
- Sepsis neonatal:
- La sepsis neonatal es una infección invasiva, por lo general bacteriana, que se produce durante el período neonatal. Los signos, que son múltiples e inespecíficos, incluyen disminución de la actividad espontánea, succión menos vigorosa, apnea, bradicardia, inestabilidad térmica, dificultad respiratoria, vómitos, diarrea, distensión abdominal, temblores, convulsiones e ictericia.
Historia.
El término σ̃ηψιζ (sepsis) es de origen griego cuyo significado era «descomposición o putrefacción de la materia orgánica animal o vegetal»; Homero, en el siglo VIII a. C. utilizó este término en La Ilíada; en el siglo IV a. C., Hipócrates lo introdujo en la Medicina.
Hipócrates consideraba que la sepsis, uno de los síndromes más antiguos y elusivos de la medicina, es el proceso por el cual se pudre la carne, los pantanos generan aire contaminado y las heridas supuran.
Tiempo después Galeno la consideró un evento loable y necesario para la cicatrización de las heridas.
En el siglo XI, Avicena utilizaba el término “pudrición de la sangre” para referirse a las enfermedades vinculadas con procesos purulentos importantes. Aunque ya se habían observado casos de toxicidad sistémica grave, el término específico para esa enfermedad —sepsis— recién comenzó a utilizarse en el siglo XIX. Hacia fines de ese siglo se creía que los microbios producían sustancias que podían enfermar al mamífero huésped y que las toxinas solubles liberadas durante la infección causaban la fiebre y el choque séptico comunes durante las infecciones graves.
En el año 1834, el término sepsis se incorporó al diccionario francés, significando putrefacción. En 1858, se incorporó al diccionario inglés, Oxford English Dictionary.
Con la confirmación de la teoría de los gérmenes por Semmelweis, Pasteur y otros científicos la sepsis se redefinió como una infección sistémica que a menudo se describía como “envenenamiento de la sangre” y se suponía que era el resultado de la invasión del huésped por microorganismos patógenos que luego se extendían por el torrente sanguíneo.
Sin embargo, con el advenimiento de los antibióticos modernos la teoría de los gérmenes pasó a ser una explicación incompleta de la patogenia de la sepsis dado que muchos pacientes con esa enfermedad morían pese a la erradicación del agente causal. Por lo tanto, los investigadores sugirieron la posibilidad de que el determinante de la patogenia fuera el huésped, no el germen.
En 1972, Lewis Thomas propuso que la respuesta del sistema inmune frente a los microorganismos durante una infección puede ser tan fuerte que se convierta en nociva para nosotros mismos. Roger Bone acuñó el término síndrome de respuesta inflamatoria sistémica (SIRS) para describir a aquellos pacientes que presentaban evidencia clínica de este fenómeno. Varios estudios clínicos se realizaron con el fin de evaluar la eficacia de diversos agentes que pudieran disminuir los efectos adversos de esta respuesta inflamatoria; sin embargo, ninguno produjo los resultados esperados.
En 1992 un panel de consenso internacional conformado por el Colegio Estadounidense de Neumonólogos (American College of Chest Physicians o ACCP) y de la Sociedad de Medicina Intensiva de los Estados Unidos (Society of Critical Care Medicine o SCCM) intentó unificar los criterios sobre la terminología empleada para designar la sepsis y sus complicaciones. Este grupo definió la sepsis como una respuesta inflamatoria sistémica a la infección y señaló que puede surgir en respuesta a múltiples causas infecciosas y que la septicemia no es una condición necesaria ni un término útil. En cambio, el panel propuso el término «sepsis grave» para describir los casos en los que la sepsis se complica con una disfunción orgánica aguda y «choque séptico» para describir a la sepsis complicada por hipotensión refractaria a la reanimación con líquidos o por un aumento en el lactato.
En 2003 un segundo panel de consenso que contó con la presencia de veintinueve participantes procedentes de Europa y América del Norte, y que conformaron cinco subgrupos para evaluar diferentes áreas, a saber, signos y síntomas de sepsis, marcadores celulares, citocinas, datos microbiológicos y los parámetros de la coagulación aprobó la mayor parte de esos conceptos, con la advertencia de que los signos de respuesta inflamatoria sistémica como la taquicardia o un recuento de leucocitos elevado se producen en muchos cuadros infecciosos y no infecciosos y por ende no son útiles para distinguir la sepsis de otras afecciones.
Epidemiología.
La sepsis provoca millones de muertes anuales en el mundo y es la causa más común de deceso entre las personas hospitalizadas.
La incidencia mundial de sepsis se estima en dieciocho millones de casos por año.
En los Estados Unidos la enfermedad afecta a alrededor de tres de cada mil personas y la sepsis grave contribuye con más de doscientas mil muertes al año.
La sepsis se observa en el 1-2 % de todas las hospitalizaciones y explica hasta el 25 % por ciento de utilización de las camas de las unidades de cuidados intensivos. Dado que rara vez se la informa como diagnóstico primario (a menudo es una complicación del cáncer o de otras enfermedades), es probable que haya una subestimación de su incidencia y de la mortalidad y la morbilidad asociadas.
Un estudio realizado por la AHRQ (Agency for Healthcare Research and Quality o Agencia para la Investigación del Cuidado y la Calidad de la Salud) de estados seleccionados reveló que en 2010 hubo cerca de 651 internaciones hospitalarias por cada 100 000 habitantes con diagnóstico de sepsis, que es la segunda causa de muerte en las unidades de cuidados intensivos no coronarias y la décima causa más común de muerte en general (la primera es la enfermedad cardíaca). La mayor incidencia de sepsis grave se observa en los niños de menos de doce meses y en los adultos mayores. Entre los pacientes estadounidenses con varios ingresos hospitalarios por sepsis en 2010, en los que después del alta de la hospitalización inicial fueron internados en un centro especializado en la atención de enfermos crónicos o de atención de largo plazo hubo más probabilidades de reinternación que en los que después del alta recibieron otra forma de atención. En un estudio que abarcó dieciocho estados de los Estados Unidos se comprobó que en 2011 entre los pacientes de Medicare la septicemia fue la segunda causa más común de reinternación dentro de los treinta días.
Varias situaciones médicas aumentan la susceptibilidad a la infección y al desarrollo de sepsis. Los factores de riesgo comunes incluyen la edad (el riesgo es mayor en los niños muy pequeños y en los ancianos), las enfermedades y los estados que debilitan el sistema inmunitario, como el cáncer, la diabetes o la asplenia, y los traumatismos y quemaduras de importancia.
Etiología.
Los síntomas de la sepsis no son causados por los microorganismos sino por productos químicos que libera el huésped. La respuesta que conduce a la sepsis puede ser activada por la infección de cualquier sitio corporal. Entre los sitios comunes en los que podría iniciarse una infección figuran el torrente sanguíneo, los huesos (sitio común en los niños), el riñón (infección de las vías urinarias altas o pielonefritis), el intestino (en general en asociación con peritonitis), las meninges (meningitis), el hígado y la vesícula biliar, los pulmones (neumonía bacteriana) y la piel (celulitis). En pacientes hospitalizados los sitios habituales de infección incluyen las vías intravenosas, las heridas quirúrgicas, los drenajes quirúrgicos y los sitios de ruptura de la piel conocidos como úlceras por presión.
Fisiopatología.
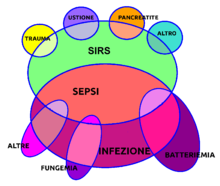
De la infección y el síndrome de respuesta inflamatoria sistémica a la sepsis. trauma: traumatismo; ustione: quemadura; pancreatite: pancreatitis; altro: otro; SIRS: síndrome de respuesta inflamatoria sistémica; sepsi: sepsis; altre: otras; fungemia: fungemia; infezione: infección; batteriemia: bacteriemia.
La sepsis es consecuencia de una combinación de factores relacionados con el patógeno invasor y con el estado del sistema inmunitario del huésped. La fase temprana de la enfermedad, caracterizada por una inflamación excesiva (que a veces desencadena una tormenta de citocinas), puede ser seguida por un período prolongado de disminución del funcionamiento del sistema inmunitario. Cualquiera de esas fases puede resultar fatal.
Patogenia.
Las enfermedades y otras situaciones que más predisponen a la aparición de sepsis por bacterias gramnegativas son la diabetes mellitus, enfermedades linfoproliferativas como la leucemia, la cirrosis hepática, las quemaduras extensas y ciertos fármacos neutropénicos. Por otra parte, la sepsis por bacterias grampositivas es más probable en asociación con catéteres intravenosos, sondas vesicales, prótesis y el uso de drogas intravenosas.
La transición de la sepsis a sepsis grave/choque séptico es consecuencia de una serie de eventos patogénicos. La reacción inicial a la infección es una respuesta neurohumoral proinflamatoria y antiinflamatoria generalizada. Ese proceso comienza con la activación de los monocitos, los macrófagos y los neutrófilos que interactúan con las células endoteliales a través de numerosos receptores de reconocimiento de patógenos. La respuesta del huésped incluye además la movilización de sustancias del plasma como resultado de esa activación celular y la alteración del endotelio. Esas sustancias plasmáticas incluyen citosinas como el factor de necrosis tumoral, interleucinas, caspasa, proteasas, leucotrienos, cininas, especies reactivas del oxígeno, óxido nítrico, ácido araquidónico, factor de activación de las plaquetas y eicosanoides. La activación del complemento y las cascadas de la coagulación amplifica aún más esta elaborada cadena de acontecimientos. El endotelio vascular es el sitio predominante de estas interacciones y, como resultado, hay lesión microvascular, trombosis y una pérdida de la integridad endotelial (fuga capilar), con la consiguiente isquemia de los tejidos. Esa interrupción difusa del endotelio es la causa de las diversas disfunciones de órganos y de la hipoxia tisular global que acompañan a la sepsis grave/choque séptico. Las terapias fundamentales que han llevado a reducir la mortalidad de los pacientes con esta patología se dirigen a revertir esos mecanismos patogénicos.
Anatomía patológica.
Diagnóstico.
La sepsis se sospecha en pacientes con fiebre y aumento del ritmo cardíaco y la frecuencia respiratoria. En esos casos a menudo se realiza un examen de sangre en busca de un número anormal de leucocitos, un signo común de sepsis, o un nivel elevado de lactato, que se correlaciona con la gravedad de la afección. También se pueden analizar la sangre y otros líquidos corporales —como la orina y el esputo— para detectar la presencia de agentes infecciosos. Además, una radiografía de tórax o una tomografía computarizada ayudarán a identificar el lugar de la infección.
Criterios diagnósticos basados en la Conferencia de Consenso de 2001.
Los criterios diagnósticos se basan en las definiciones siguientes:
El término síndrome de respuesta inflamatoria sistémica (SRIS) se refiere a la respuesta inflamatoria generalizada que se produce contra diferentes lesiones infecciosas o no infecciosas. Desde el punto de vista clínico, para diagnosticar un SRIS deben cumplirse al menos dos de los siguientes criterios:
- Temperatura >38 oC o <36 oC.
- Frecuencia cardíaca >90 latidos por minuto.
- Taquipnea >20 respiraciones por minuto o PaCO2 <32 mmHg.
- Leucocitosis >12 000 cel/mm³ o leucopenia <4000 cel/mm³ o más de 10 % de formas inmaduras.
La palabra sepsis alude a la expresión de la respuesta inflamatoria sistémica provocada por una infección, independientemente del tipo de germen (bacteria, virus, hongo o parásito) o de si el germen se encuentra en la sangre o no.
El término sepsis grave define la sepsis asociada con disfunción de órganos, hipoperfusión (acidosis láctica, oliguria y alteraciones del estado mental) o hipotensión que revierte con la administración de líquidos.
El choque séptico, que es el asociado con sepsis grave como su expresión de mayor gravedad, requiere la presencia de un SRIS de origen infeccioso más criterios de hipoperfusión e hipotensión persistente (presión arterial sistólica <90 mmHg o presión arterial media (PAM) <70 mmHg o caída >40 mmHg de la presión arterial sistólica desde la basal) que no revierten con la administración de líquidos (2 L de cristaloides en 1 hora) y por lo tanto requieren el empleo de drogas vasopresoras para su corrección.
El término síndrome de disfunción multiorgánica define la alteración de la función de al menos dos órganos o sistemas en un paciente con una patología aguda en quien la homeostasis ya no puede mantenerse sin intervención.
Criterios basados en la nueva definición de sepsis.

Diagnóstico de sepsis basado en las escalas de medición qSOFA y SOFA según la definición de sepsis-3 de febrero de 2016.
Después de la revisión de las definiciones de sepsis y choque séptico de 2001 hubo avances considerables en la biopatología (cambios en la función de los órganos, la morfología, la biología celular, la bioquímica, la inmunología y la circulación), el manejo y la epidemiología de la sepsis, lo que sugirió la necesidad de una nueva revisión destinada a evaluar las definiciones de sepsis y choque séptico anteriores y actualizarlas en caso de que fuera necesario. Por lo tanto, la Sociedad de Terapia Intensiva estadounidense y su análoga europea convocaron a un grupo de investigadores con experiencia en biopatología, ensayos clínicos y epidemiología de la sepsis para que revisaran las definiciones y los criterios clínicos vigentes en ese momento.
La sepsis no es una enfermedad específica sino un síndrome que abarca una biopatología (conjunto de alteraciones estructurales que subyacen en los procesos de enfermedad) todavía incierta que puede ser identificada por una serie de signos y síntomas clínicos en un paciente con sospecha de infección, pero ante la falta de una prueba diagnóstica de referencia los expertos convocados a la última conferencia internacional de consenso buscaron definiciones y criterios clínicos de apoyo que fueran claros y satisficieran múltiples dominios de utilidad y validez.
Según esos científicos, la falta de un criterio diagnóstico estándar, al igual que en muchas otras enfermedades sindrómicas, impide una validación inequívoca y en su lugar requiere estimaciones aproximadas del rendimiento a través de una variedad de dominios de validez, como se indicó antes. El objetivo de la revisión era ayudar al médico de cabecera, y tal vez dar lugar a una intensificación de la atención, mediante el desarrollo y la validación de criterios clínicos simples (como la escala qSOFA) para identificar a los pacientes con sospecha de infección y probabilidad de malos resultados, es decir de una internación prolongada en la unidad de cuidados intensivos y de muerte en el hospital, un enfoque con importantes implicaciones epidemiológicas y de investigación. Los criterios propuestos deberían ayudar a la categorización del diagnóstico una vez completados la evaluación inicial y el manejo inmediato.
En la opinión de los expertos las limitaciones de las definiciones previas incluían una focalización excesiva en la inflamación, el patrón engañoso según el cual la sepsis es un continuo que va de sepsis grave a choque y la falta de especificidad y sensibilidad de los criterios de SRIS. Las múltiples definiciones y las diversas terminologías en uso para aludir a la sepsis, al choque séptico y a la disfunción de órganos generaban discrepancias en la incidencia y las tasas de mortalidad informadas. El grupo de expertos llegó a la conclusión de que el término “sepsis grave” era redundante y recomendó la definición de sepsis que ya se mencionó (una disfunción de órganos potencialmente mortal causada por una respuesta no regulada del huésped a la infección). En cuanto a la disfunción de órganos, puede ser definida como un aumento de dos o más en la puntuación de la escala SOFA, que como también se dijo se asocia con una mortalidad hospitalaria superior al diez por ciento. El choque séptico se definió como una afección derivada de la sepsis en la que las anomalías circulatorias, celulares y metabólicas particularmente importantes se asocian con un riesgo de mortalidad mayor que el asociado con la sepsis sola. Como se comentó antes, los pacientes con choque séptico pueden ser identificados por la necesidad de vasopresores para mantener una presión arterial media (PAM) de 65 mmHg o mayor y un nivel sérico de lactato superior a 2 mmol/L (> 18 mg/dL) en ausencia de hipovolemia, combinación vinculada con tasas de mortalidad hospitalaria de más del cuarenta por ciento.
En ámbitos extrahospitalarios, en la sala de urgencias o en las salas comunes para internación los pacientes adultos con sospecha de infección pueden ser identificados rápidamente como más propensos a experimentar los resultados desfavorables típicos de la sepsis si satisfacen al menos dos de los criterios que juntos constituyen una nueva escala de puntuación clínica de cabecera denominada q SOFA (escala SOFA rápida): frecuencia respiratoria de 22/min o mayor, alteración del estado mental o una presión arterial sistólica ≤ 100 mmHg. La conclusión de los expertos fue que las definiciones y los criterios clínicos anteriores deben ser reemplazados por los recién actualizados que se acaban de describir para facilitar el reconocimiento temprano y el manejo más oportuno de los pacientes con sepsis o en riesgo de desarrollarla.
Otro problema importante que se consideró en las reuniones fue el de que rara vez se cuenta con la confirmación microbiológica de la infección cuando se inicia el tratamiento; además, aun cuando se hayan completado las pruebas microbiológicas, la “sepsis” con cultivo positivo se observa solo en el treinta al cuarenta por ciento de los casos. Según los miembros del grupo de expertos ni qSOFA ni SOFA van a aportar un criterio de definición único de la sepsis y es esencial que la no satisfacción de dos o más criterios de esas escalas no genere un aplazamiento de la investigación diagnóstica o el tratamiento de una infección ni un retraso en cualquier otro aspecto de la atención considerado necesario por los médicos. La escala qSOFA se puede implementar rápidamente a la cabecera del paciente sin necesidad de análisis de sangre y los investigadores esperan que facilite la rápida identificación de una infección que plantee una mayor amenaza para la vida. Si no se han llevado a cabo las pruebas de laboratorio apropiadas, esa escala puede apresurar la evaluación mediante pruebas bioquímicas para identificar disfunción de órganos. Esos datos ayudarán sobre todo al manejo del paciente, pero también permitirán la obtención posterior de la puntuación SOFA.
Los expertos que formularon las últimas definiciones subrayan que los criterios del SRIS todavía pueden ser útiles para la identificación de la infección. Además, sostienen que, aunque los datos de la escala qSOFA son menos sólidos que una puntuación SOFA de dos o más en la unidad de cuidados intensivos, esa escala no requiere pruebas de laboratorio y permite una evaluación rápida y repetida. También sugieren que se utilicen los criterios de la escala qSOFA para ayudar a los clínicos a investigar más rápido en busca de una posible disfunción de órganos, a iniciar o intensificar el tratamiento correcto y a considerar la suspensión de la terapia intensiva o el aumento de la frecuencia de monitoreo. Además, consideran que el hallazgo de criterios qSOFA positivos también debe plantear la posibilidad de una infección en pacientes en los que todavía no se la había sospechado.
Como ya se dijo, las definiciones y los criterios clínicos actualizados deben sustituir a los anteriores. En febrero de 2016 la redefinición de la sepsis aporta perspectivas nuevas en cuanto a la forma en que debe verse esa enfermedad y proporciona nuevos criterios diagnósticos por medio de la escala SOFA y la nueva escala qSOFA (SOFA rápida).
Para finalizar debe mencionarse que los científicos que reformularon la definición de sepsis y otros términos relacionados subrayaron que el proceso de actualización y redefinición no ha terminado y recomendaron que, como se hace con el software y otras actualizaciones de codificación, la nueva definición se designe sepsis 3 y las de 1991 y 2001 sean reconocidas como sepsis 1 y sepsis 2, respectivamente, para hacer hincapié en la necesidad de futuras versiones.
No obstante, cabe destacar la falta de consenso en el campo médico respecto a esta nueva definición. Múltiples autores arguyen que si bien es cierto que la definición previa basada en el SIRS no es una herramienta perfecta, su utilidad está ampliamente fundamentada. Dada la alta mortalidad de la sepsis, debiera primarse una herramienta de screening de alta sensibilidad, como ha sido el SRIS, frente a la especificidad, algo mayor con el SOFA. En múltiples estudios se ha objetivado una relación directamente proporcional entre mortalidad y el SRIS. Además, su uso, así como las definiciones de sepsis previas y las intervenciones asociadas han reducido significativamente la mortalidad global por sepsis. Por tanto, sustituir una definición de sepsis que ha supuesto una disminución global de la mortalidad, y ha bajado las cifras de sepsis grave alrededor del 7-16 % y del shock séptico del 20-25 % y que está ampliamente extendida y validada (mayor precocidad con menor mortalidad)—, por otra de uso marginal, sin estudios prospectivos en diferentes tipos de pacientes, entornos y regiones que respalden este cambio, supone un ejercicio de riesgo al que no deben exponerse los pacientes.
